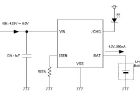
Dry Cell Electrolyser
Här är teorin: electrolyser använder olika Joniska laddningen på olika atomerna i molekylen att dela upp den i dess respektive laddade atomer eller molekyler, till exempel vatten blir uppdelad i väte och syre eftersom i vattenmolekylen vätet är något positivt laddade och syre är något negativt laddade. Dessa avgifter är endast mycket liten, + 1 elektron volt (ev) för varje väte och -2 ev på varje syreatom. Bara för jämförelse 1 elektron volt är 1,6 × 10−19 Coulomb (c) och 1 Coulomb är avgiften transporteras av en stadig ström av en ampere i en sekund. Vätet är attraherad av negativt laddade elektroden eller katod och syret lockas till positivt laddade elektroder eller anoder. På anoderna löst syrejoner en elektron och bond att formuläret syrgas, vid katoder vätejonerna få en elektron från katoden och sedan knyta an till bildar vätgas. Denna överföring av elektroner från och till elektroderna fullbordar kretsen och tillåter nuvarande att flöda. En katalysator kan användas för att göra processen mer effektiv genom att minska den energi som behövs för att starta processen. den katalysator som jag använder är sodiumhydroxide i en 1 till 40 blandning med avjoniserat vatten. Vattnet behöver inte vara avjoniserat men det förlänger livslängden på enheten som mineraler och andra saker kommer inte att bygga upp på elektroderna.